Wiadomości ogólne
- Czas trwania zajęć: 90 minut
- Pojęcia kluczowe:
- korozja,
- niszczenie,
- metale,
- stopy metali.
- Hipoteza sformułowana przez uczniów:
- Korozja jest procesem niszczenia metali.
- Korozja niekorzystnie wpływa na metalowe konstrukcje.
Doświadczenie
- Potrzebne materiały, przyrządy:
Ocet, woda destylowana, woda z kranu, sól kuchenna, kwas siarkowy(VI), 5 zlewek, cylinder miarowy, łyżeczka, 5 szkiełek zegarkowych, pinceta, papier ścierny, krystalizator, 5 stalowych gwoździ.
- Uwagi dotyczące BHP:
Doświadczenia należy wykonywać z zachowaniem odpowiednich środków bezpieczeństwa. Niezbędny jest kitel, okulary ochronne oraz rękawice.
Kwas octowy:
R10 Produkt łatwopalny.
R35 Powoduje poważne oparzenia.
S1/2 Przechowywać pod zamknięciem i chronić przed dziećmi.
S23 Nie wdychać oparów.
S26 Zanieczyszczone oczy przemyć natychmiast dużą ilością wody i zasięgnąć porady lekarza.
S37/39 Nosić odpowiednie rękawice ochronne i okulary lub ochronę twarzy.
S45 W przypadku awarii lub jeżeli źle się poczujesz, niezwłocznie zasięgnij porady lekarza — jeżeli to możliwe, pokaż etykietę.
Kwas siarkowy(VI):
R: 35; Powoduje poważne oparzenia.
S: 26-30-45; Zanieczyszczone oczy przemyć natychmiast dużą ilością wody i zasięgnąć porady lekarza. Nigdy nie dodawać wody do tego produktu. W przypadku awarii lub jeżeli źle się poczujesz, niezwłocznie zasięgnij porady lekarza - jeżeli to możliwe, pokaż etykietę.
- Zmienne występujące w doświadczeniu:
- zmienna zależna (co badamy?): powierzchnia gwoździa,
- zmienna niezależna (co zmieniamy?): rodzaj roztworu,
- zmienna kontrolna (czego nie zmieniamy?): objętości roztworów, rodzaj gwoździa, czas.
Instrukcja wykonania doświadczenia:
Zadanie A:
Etap przygotowania:
Przy użyciu papieru ściernego starannie oczyszczamy 5 gwoździ, a następnie umieszczamy je w roztworze kwasu siarkowego(VI), w celu odtłuszczenia i przepłukujemy wodą destylowaną.
Sporządzanie próbek:
I – Do zlewki wlewamy 10cm3 wody destylowanej;
II – Do zlewki wlewamy 10cm3 octu;
III – Do zlewki wlewamy 10cm3 wody z kranu;
IV – Do zlewki wsypujemy łyżeczkę soli kuchennej i wlewamy 10cm3 wody destylowanej;
V – Zlewkę pozostawiamy bez zmian.
W przygotowanych pięciu zlewkach umieszczamy stalowy gwóźdź. Odczekujemy 24h.
Etap końcowy:
Gwoździe wyciągamy i umieszczamy na odpowiednich szkiełkach zegarkowych. Obserwujemy zmiany.

Obserwacje: Gwoździe wyciągnięte ze zlewek od 1 do 4 zmieniły swój wygląd. Na ich powierzchni pojawiła się krucha substancja o barwie brązowo - rudej. Najbardziej widoczne zmiany pojawiły się po wyjęciu gwoździa ze zlewki z octem, a najmniej widoczne – po wyjęciu gwoździa ze zlewki z wodą destylowaną. Brak zmian w zlewce z powietrzem.
Wnioski: Pojawiająca się substancja o barwie brązowo-rudej to rdza, powstała m.in. z tlenków niszczonych metali. Świadczy ona o przebiegu korozji.
- Wniosek ogólny:
Korozja metali jest przykładem reakcji utleniania i redukcji. Korozja jest to proces niszczenia metali i ich stopów (stal to stop żelaza z węglem) pod wpływem czynników zewnętrznych (niezbędnym reagentem jest woda). Powstała rdza wytwarza się w reakcji żelaza z tlenem i wodą. Podczas tej reakcji powstaje trudno rozpuszczalny wodorotlenek żelaza(II) i wodorotlenek żelaza(III). Czynniki wpływające na korozję metali to: tlen z powietrza, kwaśne opady, woda słodka i słona.
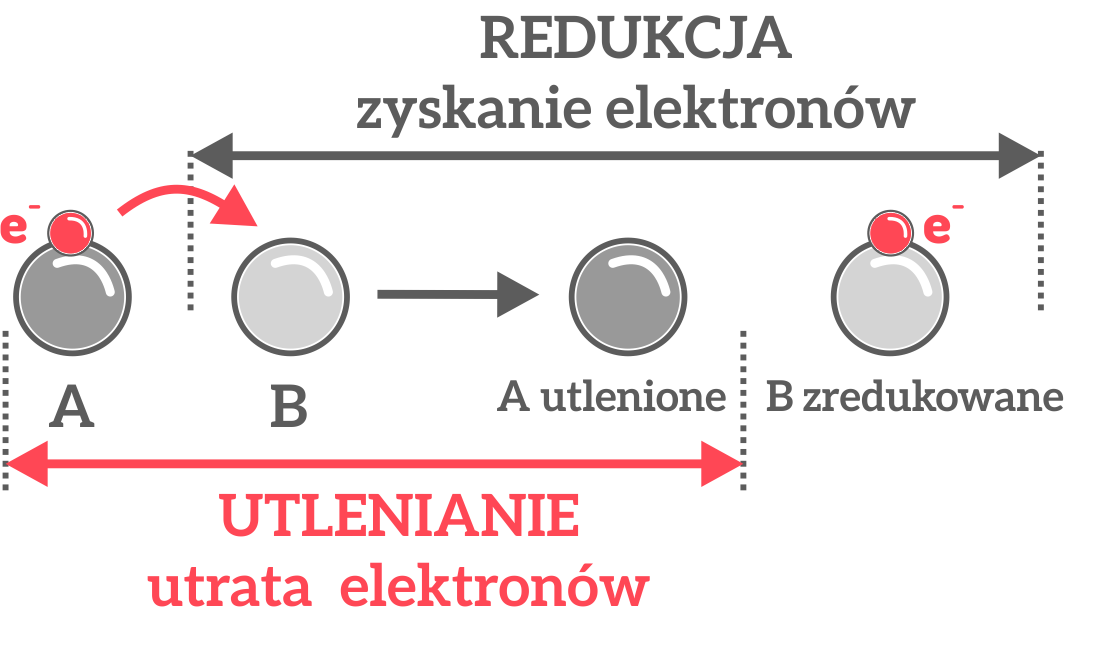
Czynnikami przyspieszającymi korozję są: gwałtowne zmiany temperatury, zakwaszenie środowiska, wilgoć, obecność niektórych soli.
- Podsumowania doświadczenia:
- Co nazywamy korozją? (Proces niszczenia metali i ich stopów pod wpływem otaczającego środowiska, prowadzące do zmiany ich właściwości).
- Jakie czynniki mogą powodować ten proces? (Tlen z powietrza, kwaśne opady, wody słodkie i słone).
- Jaki stop metali jest najczęściej wykorzystywany w przemyśle? (Stal – stop żelaza i węgla, stal szlachetna zawiera również domieszki chromu, niklu i manganu).
- Jakie czynniki przyspieszają proces korozji? (Gwałtowne zmiany temperatury, zakwaszenie środowiska, wilgoć, obecność niektórych soli).
- Jakie konsekwencje może mieć korozja w życiu codziennym? (Niszczenie metalowych konstrukcji mostów, szyn kolejowych, narzędzi).
- Czy posypywanie solą dróg może nieść jakieś konsekwencje w życiu codziennym? (Tak, może być przyczyną niszczenia karoserii samochodowych, niszczenia butów ze skóry).
Podstawa programowa
- Cele, które zostaną osiągnięte w wyniku przeprowadzenia doświadczenia przez nauczyciela i uczniów pod kierunkiem nauczyciela:
a) wymagania ogólne – cele
- uczeń wyjaśnia na czym polega proces korozji;
- uczeń wymienia czynniki wpływające na korozję.
b) wymagania szczegółowe - treści nauczania
- uczeń doświadczalnie sprawdza wpływ czynników na metal;
- uczeń wykorzystuje zdobytą wiedzę do oceny wpływu korozji w życiu codziennym;
- systematyzuje wiedzę na temat metali.
Materiały do pobrania
Słowniczek
EKSPERYMENT, prowadzony zgodnie z metodą naukową, rozumiany jest jako proces, w trakcie którego badacz, uczeń, wprowadza zaplanowaną zmianę jednego czynnika i bada, jakie ta zmiana przynosi rezultaty, uważając przy tym, by pozostałe czynniki pozostały niezmienne.
OBSERWACJA rozumiana jako zaplanowane gromadzenie faktów, bez wprowadzania jakichkolwiek ingerencji w badane zjawisko. W trakcie obserwacji nie występuje zmienna niezależna, ponieważ nie ingerujemy w badany proces.
Eksperyment i obserwacja są realizowane zgodnie z metodą naukową, a to oznacza:
Postawienie PYTANIA BADAWCZEGO - Pytanie może być zadane przez uczniów lub zaproponowane przez nauczyciela. Pozwala to ukierunkować myśli i skoncentrować się na badanym problemie, uświadamia, że badania naukowe są wynikiem zaplanowanego działania.Dobrze skonstruowane pytanie badawcze jest pytaniem otwartym - uczeń sam chce znaleźć na nie odpowiedź.
Kolejnym krokiem jest postawienie HIPOTEZY, czyli prawdopodobnej, przewidywanej i wymyślonej przez uczniów odpowiedź na pytanie badawcze. Pamiętajmy, że przed wykonaniem eksperymentu nie ma złych lub dobrych hipotez, każda, nawet najbardziej śmiała jest dopuszczalna.
Kolejny etap to określenie ZMIENNYCH:
- ZMIENNA NIEZALEŻNA czyli to, co zmieniamy.
- ZMIENNA ZALEŻNA czyli wielkość, którą będziemy mierzyć, obserwować.
- ZMIENNE KONTROLNE czyli wszystko to, co musi zostać niezmienne.
ZMIENNA ZALEŻNA to parametr mierzony podczas doświadczenia, zmieniający się w zależności od zmian ZMIENNEJ NIEZALEŻNEJ.
W doświadczeniu naukowym pojawiają się również PRÓBY KONTROLNE. Bez kontroli nie można jednoznacznie stwierdzić, czy wyniki doświadczenia są wiarygodne. Kontrola pozytywna to dodatkowa próba, którą przeprowadzamy identycznie, jak próbę badawczą, ale z użyciem takiego czynnika (jeśli jest znany), który na pewno wywołuje pożądany efekt. Z kolei kontrola negatywna to dodatkowa próba, ale bez użycia czynnika, o którym wiemy, że wywołuje badane zjawisko. Z założenia, wynikiem tej próby będzie brak zmiany mierzonego parametru. Nie w każdym układzie doświadczalnym da się zaplanować obie próby kontrolne.
Zajęcia z pytaniem problemowym zakładają dyskusję między uczniami na podstawie dodatkowych pytań lub przykładów dostarczonych przez nauczyciela. Zajęcia te kształcą umiejętność doboru i formułowania argumentów, słuchania osób o innym stanowisku oraz wyciągania wniosków. W wyniku dyskusji cenne byłoby wypracowanie stanowiska, by uczniowie przekonali się, że każda konstruktywna rozmowa powinna zakończyć się rzetelnym podsumowaniem.
Gry dydaktyczne wykorzystują czynnik zabawy, co wspomaga przyswajanie wiedzy przez uczniów. Gry rozwijają pomysłowość, aktywność, samodzielność, umiejętność pracy w grupie oraz uczą radzenia sobie z emocjami. Grając uczymy się przez działanie i przeżywanie. Sukcesem jest osiągnięcie celu, a nie wygrana z innymi, czy zajęcie pierwszego miejsca. Najważniejsza w grze jest dydaktyka. Wygrywać mają wszyscy.
Bibliografia
- Chemia w gimnazjum, WSiP, Z. Kluz, K. Łopata, Warszawa 1999.
- Chemia 1 - podręcznik dla gimnazjum, OPERON, M. Szczepaniak, B. Kupczyk, W. Nowak, Gdynia 2009.
- Chemia ogólna i nieorganiczna, Nowa Era, M. Litwin, Sz. Styka-Wlazło, J. Szymońska, Warszawa 2004.